A aprovação do lenacapavir nos EUA como PrEP injetável semestral pode revolucionar a prevenção do HIV, mas enfrenta barreiras regulatórias e econômicas para ser incorporado ao SUS no Brasil.
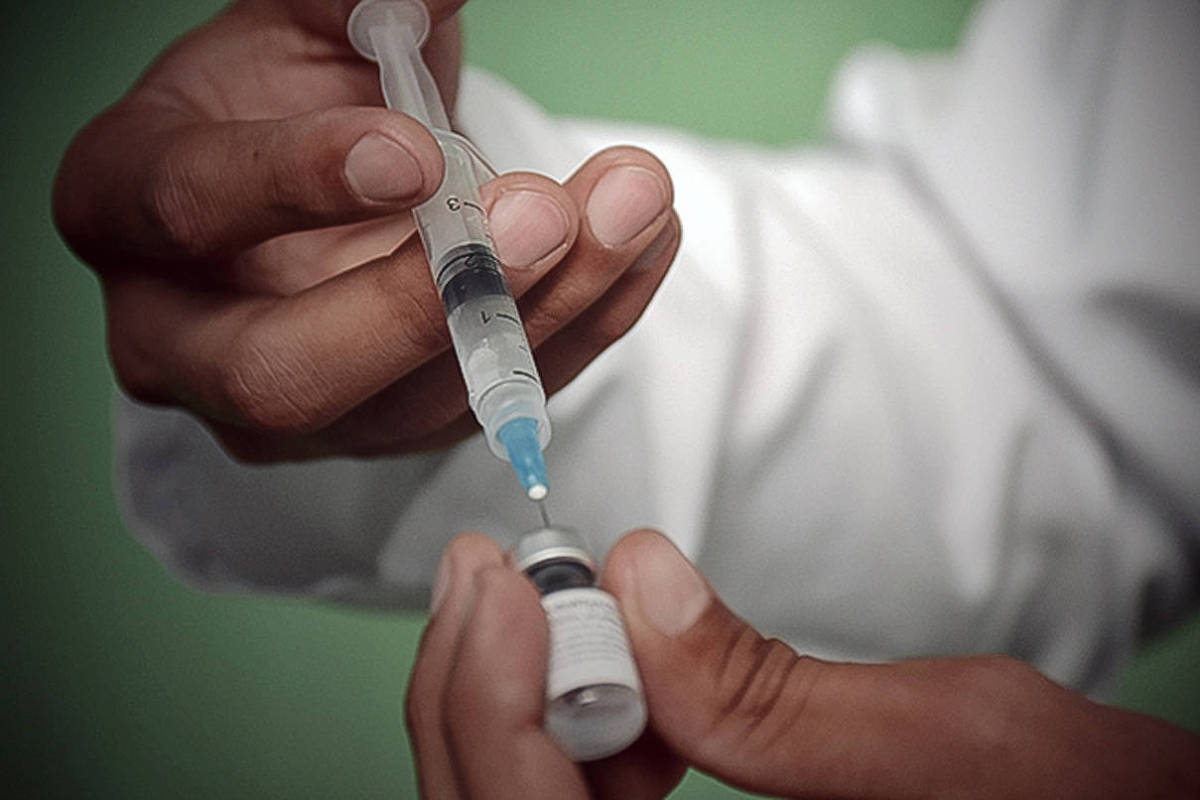
A aprovação do lenacapavir nos Estados Unidos como a primeira opção injetável de longa duração para profilaxia contra o HIV representa um avanço significativo na prevenção da infecção. Com aplicação subcutânea semestral, essa nova abordagem pode facilitar a adesão ao tratamento, especialmente entre populações vulneráveis que têm dificuldade com a PrEP oral, disponível no Brasil desde 2018. A profilaxia oral exige que o paciente tome um comprimido diariamente, o que tem gerado altos índices de abandono.
Dados do Ministério da Saúde indicam que a adesão à PrEP oral é um desafio, com muitos usuários não completando o tratamento. O lenacapavir, um inibidor de capsídeo, atua em várias etapas do ciclo de replicação do HIV e demonstrou eficácia de 100% em estudos clínicos com diferentes grupos, incluindo mulheres cisgênero africanas e homens que fazem sexo com homens. Essa nova formulação pode reduzir o estigma social associado ao uso de medicamentos visíveis contra o HIV.
Apesar do potencial do lenacapavir, sua incorporação ao Sistema Único de Saúde (SUS) enfrenta barreiras regulatórias e econômicas. O medicamento ainda não foi aprovado pela Agência Nacional de Vigilância Sanitária (Anvisa) para uso como PrEP, o que impede sua avaliação pela Comissão Nacional de Incorporação de Tecnologias (Conitec). Atualmente, existem dois pedidos de registro em análise, mas o tempo de aprovação pode ser afetado por fatores técnicos.
Além das questões regulatórias, o custo do lenacapavir é uma preocupação. Pesquisadores estimam que o custo de produção do medicamento seria de US$ 25 a 46 por pessoa ao ano, mas o preço nos Estados Unidos ultrapassa US$ 28 mil por paciente anualmente. Essa discrepância gerou pressão de entidades como o UNAIDS, que exige preços mais acessíveis, especialmente para países de renda média e baixa. A Gilead Sciences, fabricante do medicamento, firmou acordos de licenciamento com fabricantes de genéricos, mas o Brasil não está incluído.
A exclusão de países como o Brasil, que possuem sistemas de saúde pública robustos e alta carga de HIV, levanta preocupações sobre a equidade no acesso a inovações médicas. A Gilead afirma que pretende aplicar estratégias de precificação escalonada, mas ainda não apresentou propostas concretas para o Brasil. A falta de clareza sobre os custos impede o planejamento adequado dos sistemas de saúde e dificulta a discussão sobre a viabilidade de incorporação do lenacapavir no SUS.
É essencial que o Brasil atue rapidamente para acelerar a avaliação regulatória do lenacapavir e inicie um debate público sobre sua inclusão na PrEP. O governo deve buscar acordos de licenciamento e transferência de tecnologia para permitir a produção nacional. A luta contra o HIV no Brasil continua, e a inovação deve ser acompanhada por vontade política e compromisso com a equidade. Nessa situação, nossa união pode ajudar os menos favorecidos a terem acesso a tratamentos que salvam vidas.

Inaugurado o Centro de Apoio Biopsicossocial no DF, com investimento de R$ 3 milhões. O espaço inédito no Brasil visa promover a saúde mental e física dos servidores de segurança pública, com planos de expansão.

A FDA aprovou o teste de sangue Lumipulse, que detecta placas amiloides associadas à doença de Alzheimer, oferecendo uma alternativa menos invasiva e mais acessível para o diagnóstico. Essa inovação promete facilitar o diagnóstico precoce e melhorar o atendimento clínico nos Estados Unidos.

Crises hipertensivas demandam socorro imediato para prevenir danos severos à saúde. Sintomas como dor no peito e visão turva são sinais de alerta. Dieta equilibrada e exercícios são essenciais para controle da pressão arterial.

Brasil busca certificação da OPAS/OMS para eliminar transmissão vertical do HIV, com taxas abaixo de 2% e incidência em crianças abaixo de 0,5 por mil nascidos vivos. O ministro Alexandre Padilha destaca a importância dessa conquista.

Após ser diagnosticada com diabetes tipo 2, uma mulher transformou sua vida ao adotar hábitos saudáveis, resultando em perda de 25 quilos e controle da glicemia. Médicos destacam a importância da mudança.

Pesquisa Datafolha revela que 62% dos brasileiros se preocupam com a esteatose hepática, mas 24% desconhecem os métodos de diagnóstico. A falta de informação pode levar a crenças em tratamentos não comprovados.